支持 I 期临床项目

先进疗法开发商的临床 I 期解决方案
为您的首次人体试验提供可扩展、合规的供应链支持
I 期试验是您的疗法从概念走向患者护理的关键里程碑,这意味着出错的余地消失了。每一批货物、每一道工序、每一个决定……您所做的一切都需要保护患者安全,坚持监管标准。Cryoport Systems 从最初阶段就与您合作,为您提供符合 IND 要求并可在全球范围内扩展的供应链,现在的设计是为了以后阶段的连续性。我们的集成式端到端供应链平台消除了各自为政的现象,减轻了运营负担,让您专注于科学研究,而我们则负责管理复杂性。
我们拥有完全自有的运输车队、综合状态监控和 ISO 21973 认证流程,可确保您的材料在每一英里范围内都得到保护。从低温保存白血球生成起始材料,到用于样本采集和制造的定制试剂盒,我们的解决方案可实现工作流程标准化并降低风险。与 Cryoport Systems 合作,您将获得一个了解利害关系的合作伙伴,让您对首批患者和未来的每一个里程碑充满信心。
您的临床供应链,为第一阶段的成功而打造
保护患者、加快发展的全面解决方案
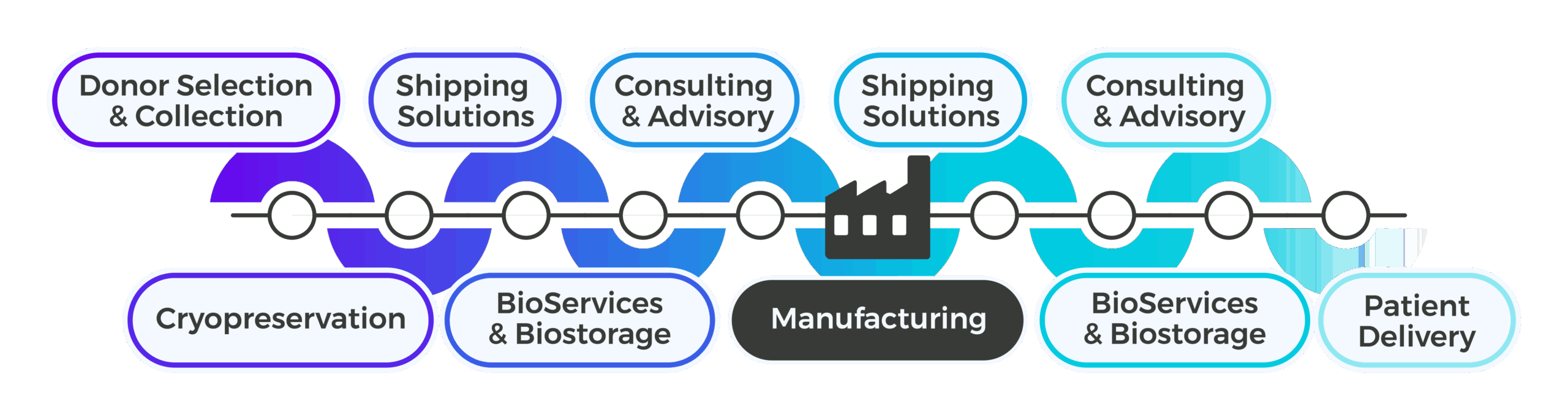
支持上游制造
在首次患者注册前建立标准化流程
I 期试验要求上游战略能够预见监管审查和未来的可扩展性。Cryoport Systems 与您合作,设计与 GMP 一致的流程和工作流程,以消除可变性并确保各生产基地的可重复性。我们的专家帮助您实现白细胞采集和试剂盒生产的标准化流程,降低风险,避免在生产过程中出现代价高昂的返工。通过及早整合低温保存和生物贮存规划,您可以在生产和患者交付之间架起一座无缝的桥梁。全球设施访问和跨地区统一程序使您能够支持多站点试验,而不会影响合规性。
- 符合 GMP 和 ISO 21973 标准,才会有第一个病人
- 用于收集和制造的标准化试剂盒设计
- 端到端集成,包括低温保存、物流和生物储存
- 全球设施访问,支持多站点试验
- 为主动降低风险和监管备案提供咨询支持
早期试验不容许出现效率低下或合规漏洞。通过与 Cryoport Systems 合作,您将获得一个供应链基础,它能预见 IND 的要求,并能随着项目的发展而无缝扩展。我们的上游战略可消除各生产基地之间的差异,减轻运营负担,并防止开发后期代价高昂的返工。这种积极主动的方法意味着您的团队可以专注于患者注册和科学里程碑,而我们则能确保每个流程都是标准化的,并可随时进行审计。有了 Cryoport Systems,上游规划将成为一种战略优势,加速您进入第二阶段及以后的发展。
支持下游制造
首次人体试验的安全运输
生产完成后,下游物流将成为临床项目的生命线。Cryoport Systems 提供经过验证的运输系统、Smartpak™ 状态监测和 Chain of Compliance® 跟踪,以确保每次运输都符合监管标准。我们全资拥有的运输系统车队消除了容量限制,而 Veri-Clean® 净化和行业领先的重新认证流程则保证了每次使用的运输完整性。ISO 21973 认证流程和基于风险的通道选择减少了可变性,并保护了时间安排。Cryoshuttle® 增加了第一英里和最后一英里的快速本地交付,为敏感材料增加了另一层保护。
- 集成的Smartpak™可在整个运输过程中持续监控每批货物
- Chain of Compliance®(合规链®)可提供审计就绪数据,为 IND 做好准备
- 每次使用前对每个运输系统进行 Veri-Clean® 净化和重新认证
- 通过 ISO 21973 认证的工作流程和工艺,实现行业领先的合规性和质量
- Cryoshuttle® 可在部分地点提供专门的本地取货和送货服务
第一阶段的下游物流至关重要。每一批货物都代表着不可替代的患者材料,延误或偏差都会危及试验的完整性。Cryoport Systems 提供经过验证的框架,将经过验证的设备、持续监控、主动风险缓解以及生物服务和生物储存等关键服务结合在一起,使您的项目步入正轨。我们的综合方法可减少交接工作,并通过审计就绪的文档确保全面的可视性,从而为您的团队减少压力和不确定性。与 Cryoport Systems 合作可让您放心,您的病人就绪材料将由一支完整的专家团队负责,并有数十年的成功记录作为后盾。
保护起始材料的低温冷冻技术
标准化白细胞介导疗法,实现一致性和规模化
第一阶段的低温保存对于保持细胞完整性和疗效至关重要。Cryoport Systems 的 IntegriCell® 解决方案提供经过验证的方案和专家指导,以确保不同生产基地和批次的一致性。通过尽早实施我们的自动化封闭流程,您可以减少变异性,并顺利将技术转移到 GMP 环境中。我们的团队支持工艺验证和设备选择,确保合规性和可重复性。
- 经过验证的白血球生成起始材料冷冻保存规程
- 专有的、经过验证的自动封闭流程,实现行业领先的一致性
- 无缝 GMP 整合
- 提高样品的完整性和存活率
起始材料是治疗的基础,其完整性不容有失。Cryoport Systems 可帮助您实施低温保存策略,保护生命力,并使所有试验基地的流程标准化。这种一致性可降低风险,提高可重复性,并随着规模的扩大提高可制造性。通过在第一阶段建立这些保障措施,您可以避免代价高昂的中断,并确保患者安全不受影响。
临床试验综合生物服务
收集、储存和管理标准化
I 期试验需要精确协调样本的采集、储存和管理。Cryoport Systems 的生物服务提供符合 GMP 要求的生物储存,并结合标准化的样本采集包和生产包,以减少不同试验点之间的差异。我们的临床样本管理能力可确保整个试验生命周期的全面可追溯性和完整性。凭借全球设施和持续监控,您可以确信每个样本都符合合规标准。
- 全球范围内的 GMP 生物储存设施
- 标准化的样本采集工具包和制造工具包可减少差异
- 临床样本管理的全生命周期监督
- 持续监测和审计就绪文件
- 综合物流和低温保存支持
在第一阶段,跨多个地点的样本管理很快就会变得复杂且容易出错。Cryoport Systems 通过提供集成的生物服务,从一开始就实现了采集、储存和处理的标准化,从而简化了这一难题。我们的解决方案可减少变异性,维护监管链,同时为监管部门提交文件提供审计就绪文件。这种控制水平既能确保患者安全,又能加快试验进度。有了 Cryoport Systems,生物服务将成为一项战略资产,在每一个里程碑上为您的项目提供支持。
获得 IND 和 I 期成功的专家指导
驾驭复杂的监管和运营问题
第一阶段引入了新的复杂性,从监管要求到多站点协调。Cryoport Systems 的咨询和顾问服务可提供战略性见解,帮助您规划可扩展性、合规性和风险缓解。我们的专家与您的团队合作,主动降低常见风险,选择最佳运输路线,并预测监管期望。我们还提供美国食品及药物管理局要求的运输风险评估、航道资格认证和包装验证,为您的商业跑道预先扫清障碍。
- 基于风险的物流规划
- FDA 要求的风险评估和车道资质
- 包装验证,为 IND 做好准备
- 全球项目经验的启示
第一阶段是监管期望开始影响运营现实的阶段。Cryoport Systems 通过积极的规划和专家指导,帮助您应对这一复杂局面。我们的咨询和顾问服务可减少不确定性,防止出现合规缺口,使您的项目顺利进入后期阶段。通过利用我们在数以千计的先进治疗项目和超过一百万次的成功交付中积累的经验,您将获得一个了解早期阶段物流的细微差别并提供符合您需求的解决方案的合作伙伴。
经过验证的 I 期试验运输解决方案
自信、合规地交付
运送病人准备好的材料需要精确和可靠。Cryoport Systems 拥有一支由经过验证的运输车队,专门用于低温、超低温、冷藏和受控室温运输。每次使用前,每个运输箱都要经过 Veri-Clean® 净化和完整运输系统的重新认证,确保每次运输的合规性和安全性。我们的持续监控和 Chain of Compliance® 合规链跟踪为您提供全面的可视性和审计就绪文件。通过 ISO 21973 认证的流程和基于风险的通道选择,您可以相信您的材料将完好无损地准时到达。
- 业内最大的完全自有运输系统船队
- 为生命科学量身定制的运输解决方案
- Veri-Clean 净化和再净化流程
- 持续状态监测和审计就绪文件
- 通过 ISO 21973 认证的流程和行业领先的质量标准
- 支持患者扩展的基于风险的车道选择
第一阶段的每一次运输都携带着不可替代的患者材料,因此不能出现故障。Cryoport Systems 提供的运输解决方案结合了经过验证的设备、严格的净化和再净化流程,以及集成的持续监控,在每一个环节保护您的治疗。我们的集成流程和 Cryoportal® 物流管理系统提供透明度和合规性保证,降低风险,加快决策。选择 Cryoport Systems,您就拥有了一个支持患者安全和加速成功之路的物流框架。
每个步骤都符合规定
保护患者安全和计划完整性
遵守法规和降低风险是第一阶段成功的关键。Cryoport Systems 将质量融入从低温保存到生物储存和运输的每一个流程。我们的 ISO 21973 认证、Chain of Compliance® 跟踪和持续监控为审核准备工作提供了强有力的框架。通过尽早实施基于风险的策略,您可以避免代价高昂的延误,并确保试验阶段的顺利进行。
- 通过 ISO 21973 认证的流程
- 合规链® 审计跟踪
- 持续监测,确保患者安全
- 主动发现和解决问题
第一阶段的合规性和风险管理可保障患者安全和项目信誉。Cryoport Systems 将质量和风险缓解融入供应链的每一个环节,确保审核准备就绪和运营连续性。我们积极主动的方法可在潜在问题影响时间表之前将其识别出来,从而减少团队的压力和不确定性。有了 Cryoport Systems,合规性将成为一种竞争优势,加速您获得批准的进程。
特色资源

海报展示
使用自动封闭系统进行低温处理的白细胞清除术
本海报演示视频展示了自动化、标准化和数据驱动的工作流程如何帮助您减少变异性并建立对细胞治疗计划的信心。从标准化低温保存到集成供应链解决方案,Cryoport Systems 正在 Enabling the Outcome™ 中为您的先进疗法计划提供未来保障。

文章
利用灵活、可扩展的细胞库保护生物制剂的基础
对于任何生物治疗项目来说,细胞库都是生产过程的基础。主细胞库 (MCB)、工作细胞库 (WCB) 和研究细胞库 (RCB) 代表着多年的开发工作和知识产权。它们是不可替代的资产,这些资产的安全性直接关系到…

文章
更聪明地扩大规模:全球供应链中心如何放大 CGT 计划的增长
细胞和基因治疗 (CGT) 计划是生命科学领域最复杂、最敏感的操作之一。从低温保存和生物贮藏到物流和监管合规,供应链中的每一步都会影响产品的完整性、临床时间表以及产品的可扩展性……
与 Cryoport Systems 一起启动您的 I 期临床供应链,建立一个可扩展、完全合规的战略,为未来的每个阶段做好准备。
Cryoport Systems 正通过我们无与伦比的供应链平台实现 Enabling the Outcome™。
提供全面稳健的供应链管理解决方案和值得信赖的物流服务。
Cryoport Systems 由一支致力于通过专业物流支持为生命科学服务的博士团队创建。 如今,我们的合作能力已超越物流,发展成为一个强大的供应链解决方案平台,为生命科学研究、开发和制造过程的每个阶段提供支持。 我们全面的解决方案平台使 Cryoport Systems 成为能够支持温控供应链各个方面的独立供应商。






