支持 III 期临床项目

可扩展、合规并可商业化的 III 期临床试验支持
与 Cryoport Systems 合作,利用专为可扩展性而构建的端到端供应链平台,简化复杂性并保护您的关键试验
III 期试验是临床开发中要求最高的阶段,其操作复杂性和监管审查达到了顶峰。申办者面临着扩大患者群体、启用多个全球研究机构以及在每个流程中保持绝对一致性和合规性的挑战。在这一阶段,分散的供应链和供应商过渡会带来代价高昂的延误和合规风险,从而危及时间表和 BLA 批准。Cryoport Systems 通过与单一供应商合作,将供应链的每一个关键环节整合到一个统一的平台上,从而消除了这些风险。
我们的解决方案旨在预测下游需求,确保您的 III 期业务无缝过渡到商业化,不会出现返工或中断。通过我们全球网络的标准化流程和 ISO 21973 认证的工作流程,我们可提供可重现性和审计就绪的文件,并大规模降低风险。通过与 Cryoport Systems 合作,您将获得一个致力于保护患者安全和加快时间进度的战略盟友,从而确保您的商业化进程。
全面的端到端支持
适用于供应链各个阶段的统一平台
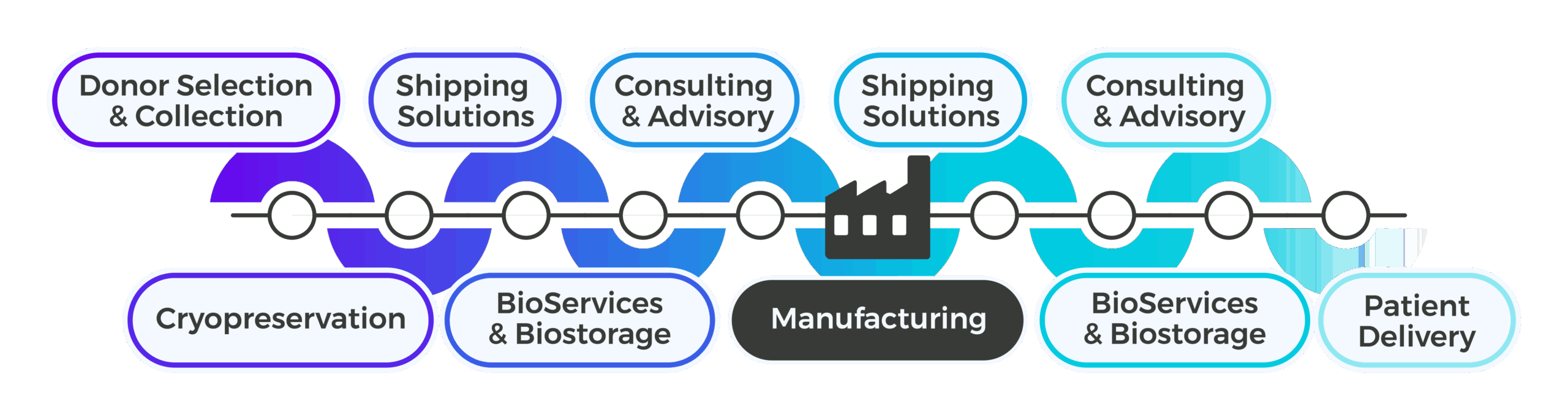
支持上游制造
简化早期阶段的复杂性,保护下游的可扩展性
第三阶段的成功始于上游的精确性。申办者往往低估了早期阶段的变异性对大规模试验的影响,导致生产和分销效率低下。Cryoport Systems 将标准化和合规性融入上游流程,包括试剂盒设计、低温保存策略和生物贮藏规划,从而降低了这些风险。我们的专家与您的团队合作,确保所有生产基地保持一致,从而减轻运营负担,消除日后知识转移的需要。通过利用我们的集成平台,您可以获得从采集到生产的连续性,并得到经过验证的工作流程和基于风险的规划的支持。这种积极主动的方法可以保障时间安排,使您的项目无缝进入商业化阶段。
- 定制试剂盒设计和生产,实现一致的样品采集
- GMP 准备就绪的综合生物贮存解决方案
- 保持材料完整性的冷冻保存策略
- 基于风险的物流规划,预测下游需求
上游精确性是第三阶段可扩展性的基础。通过尽早与 Cryoport Systems 合作,您可以消除可能影响试验完整性和监管信心的变数。我们的解决方案可降低复杂性和风险,创建一个支持每个里程碑的统一框架。这种控制水平可确保您的关键试验顺利进行,商业化道路畅通无阻。有了 Cryoport Systems,上游规划将成为成功的催化剂。
支持下游制造
通过标准化流程和全球覆盖加快时间进度
随着 III 期试验的扩大,下游操作也变得越来越复杂。申办者必须管理大规模分销,在多个地区保持合规性,并为商业化上市做好准备,而所有这一切都不能牺牲精确性。Cryoport Systems 通过单一供应商平台提供连续性,该平台将物流、生物储存、二次包装和标签整合在一个屋檐下。我们的全球网络确保接近患者群体,缩短运输时间,降低风险。我们的所有设施均采用标准化的 SOP 和 ISO 认证的工作流程,因此我们的规模化运营具有行业领先的可重复性和可审计性。我们的专家提供个性化咨询,使下游流程与监管期望保持一致,确保为 BLA 提交和商业化做好准备。
- 全球物流网络实现高效的试验覆盖
- 通过 ISO 21973 认证的工作流程,确保合规性
- Chain of Compliance®(合规链®),实现完全可追溯性,并为审计做好准备
- 在选定地点通过 Cryoshuttle® 服务快速进行本地交付
- 综合生物服务和生物储存,以确保连续性
- 合格人员 (QP) 和监管支持,以便向欧盟发布产品
下游操作是赢得或失去时间的关键。Cryoport Systems 提供基础设施和专业知识,让您的项目顺利进行。我们的解决方案可降低变异性,保护患者材料,同时确保每个接触点都合规。与我们合作,您将获得战略优势,加快进度并确保您的商业化之路。有了 Cryoport 系统,下游的复杂性将变成一个可控、可预测的过程。
为保持一致性和规模而进行低温保存
保护全球试验完整性的标准化解决方案
在 III 期试验中,起始材料的低温保存对于保持材料的完整性至关重要,因为材料的多变性会影响患者的安全和监管机构的信心。Cryoport Systems 通过我们的 IntegriCell® 平台提供标准化的低温保存解决方案,旨在确保所有研究机构和阶段的一致性。我们的自动化封闭流程可降低污染风险并保持可重复性,从而实现无缝扩展,满足大量患者的需求。通过尽早实施这些解决方案,申办者可避免因分散的低温保存策略而造成的混乱。我们的专家会就最佳实践和合规性调整提供指导,在整个供应链中保护您的材料,延长关键起始材料的可制造性,同时保持细胞活力。Cryoport Systems 与综合生物储存和验证物流相结合,创建了一个统一的框架,从采集到商业化的整个过程都能保证完整性。
- 自动化封闭式冷冻保存流程,确保一致性
- 符合 GMP 要求的综合生物储存
- 基于风险的监测和记录,为审计做好准备
- 支持全球试验扩展的可扩展解决方案
低温保存白细胞生成起始材料是第三阶段取得成功的战略差异化因素。Cryoport Systems 可确保每个样本都得到精确保存,减少变异性,保护患者安全,同时提高可制造性,并提供一体化生物储存,将冷冻保存的材料及时运送到生产厂家。我们的标准化解决方案可实现跨站点、跨阶段的连续性,使可扩展性不受影响。与我们合作,您将获得信心,相信您的材料将在整个试验生命周期内保持完整性。
提高运营效率的生物服务
通过集成生物服务和生物存储简化复杂性
III 期试验要求规模化的运营效率,而分散的生物服务会带来延误和合规风险。Cryoport Systems 将试剂盒生产、二次包装和贴标、临床样本管理、生物储存和物流整合在一个平台上,从而消除了这些难题。我们的专家会根据您的试验要求设计和生产定制的采集和制造试剂盒,确保所有试验点的一致性。通过在单一供应商关系中管理这些流程,我们减轻了运营负担,消除了多次交接的需要。我们的生物储存设施符合 GMP 标准,为敏感材料提供安全、合规的存放场所,并提供持续监控和审计文件支持。我们的合格人员(QP)和监管支持可实现全球扩张,并将药品投放到欧盟。这种整合水平可简化工作流程、加快时间进度,并使您的项目顺利进入商业化阶段。
- 定制试剂盒设计和生产,满足特定试验需求
- 符合 GMP 标准的生物储存解决方案,确保材料完整性
- 发布合格人员 (QP) 以扩展欧洲市场
- 实现端到端连续性的综合物流
- 持续监测和记录,确保合规
- 基于风险的规划,以预测未来的可扩展性
生物服务是提高 III 期试验运行效率的支柱。Cryoport Systems 在一个统一的平台上提供这些服务,降低了复杂性,保障了合规性。我们的解决方案为每个接触点创造连续性,使申办者能够专注于科学而非供应链管理。与我们合作,您将获得战略优势,加快进展并保护患者安全,将生物服务转化为成功的驱动力。
为战略调整提供咨询和顾问支持
专家指导,驾驭复杂性,确保合规性
III 期试验带来了监管和运营方面的挑战,需要专家的指导。Cryoport Systems 提供咨询和顾问服务,旨在使您的供应链战略符合全球合规标准和商业准备。我们的专家与您的团队合作,制定风险缓解计划和连续性战略,预测未来需求。通过尽早采用这些做法,申办方可避免代价高昂的返工,并保持获得 BLA 批准的势头。我们的咨询服务不仅限于物流,还包括对监管要求、进出口合规性和全球可扩展性最佳实践的深入了解。这种积极主动的方法可确保您的供应链保持弹性、合规并为商业化做好准备。
- 国际航线和复杂航线基于风险的车道资格认证
- 包装验证符合全球监管标准
- 商业跑道规划和合规准备
- 从数以千计的先进疗法项目中获得战略洞察力
在复杂的 III 期试验中,咨询和顾问服务至关重要。Cryoport Systems 提供专业知识和远见卓识,使您的项目步入正轨并符合要求。我们的解决方案可减少不确定性,降低风险,并为商业化开辟一条清晰的道路。与我们合作,您将获得信心,相信每项决策都能支持长期的成功。
提高可靠性和控制性的运输系统
经过验证的解决方案可在每一公里范围内保护患者材料
III 期试验需要大规模可靠的运输系统。Cryoport Systems 提供经过全面验证的解决方案,旨在保持每次运输过程中的材料完整性。我们的车队支持所有温度段,包括低温、超低温和受控室温,确保与任何治疗类型兼容。每个系统都配备了 Smartpak™ 状态监测技术,用于持续监测,并与我们的 Cryoportal® 物流管理平台集成,实现全面可视。这种积极主动的方法能够在出现偏差时迅速干预,保障患者材料和试验的完整性。结合我们的 Veri-Clean® 净化和每次使用前对每个运输系统的全面重新验证流程,以及完整的 Chain of Compliance® 文件,Cryoport Systems 可提供无与伦比的控制和可审计的透明度。我们的解决方案可减少变异性、降低风险,并确保每次运输都符合最高的质量和合规标准。
- 适用于所有温度带和治疗类型的多样化机群
- 用于连续监测的 Smartpak™ 状态监测技术
- 用于可视性和报告的 Cryoportal® 物流管理平台
- Veri-Clean® 净化和重新认证,确保系统完整性
- Chain of Compliance®(合规链®),实现完全可追溯性,并为审计做好准备
运输系统是 III 期试验的生命线,可靠性不容忽视。Cryoport Systems 提供集技术、合规性和可扩展性于一体的解决方案,可在每一公里范围内保护患者材料。我们的集成平台可减轻操作负担,并提供监管信心所需的透明度。与我们合作,您将获得对试验最关键环节之一的控制权。
降低风险的质量与合规性
采取积极主动的策略,保障时间安排和监管信心
III 期试验是在严格的监管审查下进行的,合规方面的漏洞可能会破坏试验的进展。Cryoport Systems 通过将质量和合规文化融入每个流程来降低这些风险。我们通过 ISO 21973 认证的工作流程、Chain of Compliance® 文件和持续监控技术,确保每批货物都符合严格的标准。我们提供审计就绪的报告和基于风险的规划,以预测和预防中断,防患于未然。我们的专家与您的团队合作,制定符合 GMP 和全球监管要求的战略。这种积极主动的方法减少了不确定性,保障了时间表,并为您的项目成功商业化奠定了基础。有了 Cryoport 系统,合规性将成为信心的源泉,而不是担忧。
- 通过 ISO 21973 认证的工作流程,符合全球标准
- Chain of Compliance®(合规链®),实现完全可追溯性和审计就绪性
- 主动降低风险的持续监测技术
- 基于风险的规划,以预测和预防干扰
质量和合规性是第三阶段成功的基石。Cryoport Systems 提供的解决方案可保护患者安全,维持监管机构的信心,最终加快商业化进程。即使面对复杂的情况,我们的前瞻性战略也能降低风险,开辟清晰的前进道路。通过与 Cryoport Systems 合作,您可以确保每个流程都符合最高标准。
特色资源

文章
超越包装盒:航运系统资质为何对先进疗法至关重要
对于先进的治疗物流而言,质量并不局限于生产车间内部。 它贯穿整个供应链,从包装和运输到在每次交接时保障材料完整性的系统。 然而,其中一个最关键的步骤(往往被低估)…

文章
更聪明地扩大规模:全球供应链中心如何放大 CGT 计划的增长
细胞和基因治疗 (CGT) 计划是生命科学领域最复杂、最敏感的操作之一。从低温保存和生物贮藏到物流和监管合规,供应链中的每一步都会影响产品的完整性、临床时间表和…
与 Cryoport Systems 一起启动您的 III 期临床供应链,建立一个可扩展、完全合规的战略,为未来的每个阶段做好准备。
Cryoport Systems 正通过我们无与伦比的供应链平台实现 Enabling the Outcome™。
提供全面稳健的供应链管理解决方案和值得信赖的物流服务。
Cryoport Systems 由一支致力于通过专业物流支持为生命科学服务的博士团队创建。 如今,我们的合作能力已超越物流,发展成为一个强大的供应链解决方案平台,为生命科学研究、开发和制造过程的每个阶段提供支持。 我们全面的解决方案平台使 Cryoport Systems 成为能够支持温控供应链各个方面的独立供应商。






